Varianta 1
Examenul de bacalaureat sesiunea august 2012
Proba E. d)
Proba scrisa la fizica
Filiera teoretica - profilul real, Filiera tehnologica - profilul tehnic si profilul resurse naturale si protectia mediului,
Filiera vocationala - profilul militar
Sunt obligatorii toate subiectele din doua arii tematice dintre cele patru prevazute de programa, adica: A. MECANICA,
B. ELEMENTE DE TERMODINAMICA, C. PRODUCEREA SI UTILIZAREA CURENTULUI CONTINUU, D. OPTICA
Se acorda 10 puncte din oficiu.
Timpul efectiv de lucru este de 3 ore.
Se considera: numarul lui Avogadro
N
A = 6,02·10
23mol
-1, constanta gazelor ideale
R = 8,31j/mol·K. Intre parametrii de stare ai gazului ideal intr-o stare data exista relatia: p·V = ν·RT.
I. Pentru itemii 1-5 scrieti pe foaia de raspuns litera corespunzatoare raspunsului corect.
(15 puncte)
1. Intr-o comprimare adiabatica a unei cantitati de gaz ideal, acesta:
a. primeste lucru mecanic si temperatura gazului scade;
b. cedeaza lucru mecanic si temperatura gazului creste;
c. primeste lucru mecanic si temperatura gazului creste;
Raspuns: Q = ΔU + L = 0; ΔU = - L, sau νC
V(T
1 - T
2 = - L,
rezulta ca T
2 > T
1 si L < 0. → c. 3p
d. primeste lucru mecanic si temperatura gazului ramane constanta. (3p)
2. Simbolurile unitatilor de masura fiind cele utilizate in manualele de fizica, unitatea de masura in S.I. a
energiei interne a gazului ideal este:
a. W b. J·s
-1 c. J·K d. J (3p)
Raspuns: [U]
SI = J. → d. 3p
3. Numarul de molecule continute in 180 ml de apa (μ
apa = 18g/mol, ρ
apa = 10
3kg/m
3 ) este egal cu:
a. 6,02·10
22 b.6,02·10
23 c. 6,02·10
24 d. 6,02·10
25 (3p)
m = ρ·V.....N
μ...............N
A
N = ρ·V·N
A/μ, N = 6,02·10
24 c. 3p)
4. Simbolurile marimilor fizice fiind cele utilizate in manualele de fizica, caldura specifica la volum constant a
gazului ideal poate fi scrisa sub forma:
a. C
V·μ
-1 b. C
V·μ c.
C
V·ν
-1 d. C
V·ν (3p)
Raspuns: C
V·μ
-1 a. 3p
5.
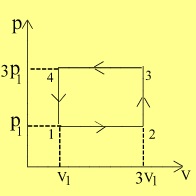
O cantitate de gaz ideal evolueaza dupa procesul ciclic 1- 2 - 3 - 4 -1 reprezentat
in coordonate p - V in figura alaturata. Relatia corecta dintre energiile interne ale
gazului corespunzatoare starilor prin care trece, este:
a. U
1 = U
4;
b. U
2 = U
4;
c. U
1 = U
2;
d. U
3 = U
2 (3p)
Raspuns: U
1 = ν·C
V·T
1; U
2 = ν·C
V·T
2;
U
3 = ν·C
V·T
3;p
1·V
1/R;U
4 = ν·C
V·T
4; p
1·V
1 = ν·R·T
1 ν·T
1 = p
1·V
1/R;
U
1 = C
V·p
1·V
1/R; U
2 = 3·C
V·p
1·V
1/R; = 3·U
1;
U
3 = 9·C
V·p
1·V
1/R; = 9·U
1; U
4 = 3·C
V·p
1·V
1/R; = 3·U
1;
→ U
2 = U
4; b. 3p.
II.
Rezolvati urmatoarea problema:
(15 puncte)
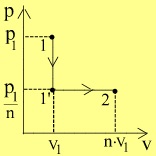
O masa m
1 = 8 g de heliu, avand masa molara μ
He = 4·10
-3kg·mol
-1, se afla la presiunea
p
1 = 2·10
5 Pa si temperatura T
1 = 400 K . Heliul, asimilat unui gaz ideal, este racit la volum constant astfel incat presiunea
lui scade de n ori. Gazul este supus apoi unui proces in care volumul sau creste de n ori la presiune
constanta. Lucrul mecanic schimbat de gaz cu mediul exterior in cele doua transformari este L
11'2 = 4986 J .
Determinati:
a. masa unei molecule de heliu;
μ......N
A
m
o.....1; m
o = μ
He/N
A 2p.
m
o = 4·10
-3kg·mol
-1/
6,02·10
23mol
-1 = 0,664·10
-26kg 2p.
b. volumul ocupat de heliu in starea initiala;
p
1·V
1 = ν·R·T
1 3p.
V
1 = m
1·R·T
1/μ·p
1
V
1 = 8·10
-3kg·8,31·10
3j/mol·400K/
4·10
-3kg·mol
-1·2 ·10
5Pa =
= 33,24·10
-3m
3. 1p
c.
temperatura heliului la finalul racirii la volum constant;
p
1/T
1 = p
1/n·T
2; T
2 = T
1/n
L
11'2 = L
11' + L
1'2; 1p.
L
11'2 = L
1'2 = (p
1/n)(n·V
1 - V
1); 1p.
n = 1/[1 - L
1'2/p
1·V
1] = 4. 1p.
T
2 = 100K. 1p.
d. densitatea heliului la finalul destinderii la presiune constanta.
ρ = m/V
3; 2p. V
3 = 3·V
1; 1p.
ρ ≅ 0,06kg/m
3. 1p.
III.
Rezolvati urmatoarea problema:
(15 puncte)
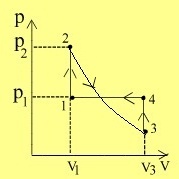
Un mol de gaz ideal monoatomic, avand caldura molara izocora 1,5 C
V = 1,5·R ,
evolueaza dupa procesul 1-2-3-4-1, reprezentat in sistemul de coordonate p - V in
graficul alaturat. Lucrul mecanic schimbat de gaz pe parcursul acestui proces este
nul. In procesul
2-3 temperatura este constanta, iar
V
3 = e
2· V
1 ( e
2 ≅ 7,4 , e fiind
baza logaritmului natural). Temperatura in starea de echilibru termodinamic 1 este
T
1 = 300 K .
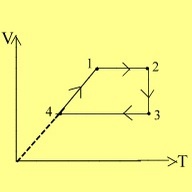
a. Reprezentati transformarea ciclica in sistemul de coordonate V-T; 4p.
b. Calculati valoarea caldurii schimbate de gaz cu exteriorul pe parcursul unui ciclu;
c. Determinati valoarea temperaturii gazului in starea 2;
Q = Q
12 + Q
23 + Q
34 + Q
41 = 0; 1p.
C
p = C
v + R;
ν·Cv·T2 -
ν·Cv·T1 + ν·R·T
2·lnV
3/V
1 +
ν·Cv·T4 -
ν·Cv·T2 +
ν·Cv·T1 -
ν·Cv·T4 + ν·R·T
1 - ν·R·T
4= 0
T
2·lne
2·V
3/V
1 + T
1 - T
4 = 0 1p.
T
2 = [T
1/2]·(e
2 - 1); 1p.
T
2 = 150K·6,4 =960K. 1p.
d. Calculati variatia energiei interne in procesul 1-2.
ΔU = ν·C
V·(T
2 - T
1) 2p.
ΔU = 8102,25J. 1p.













